

Anzeige: Amgen GmbH
Dies ist ein Angebot unseres Content-Partners*, Amgen GmbH, der für diesen Inhalt verantwortlich ist.
Vectibix® als Erstlinientherapie bei RAS-Wildtyp-mCRC-Patient:innen*,1:


40 Monate medianes Gesamtüberleben in ausgewählten Subgruppen2-6
Mit Vectibix® konnte ein medianes Gesamtüberleben (mOS) von 40 Monaten in ausgewählten Subgruppen nachgewiesen werden.2-6 Unter anderem in der Biomarkeranalyse der prospektiven Phase-III-Studie PARADIGM ergab sich unter Vectibix® ein verlängertes Gesamtüberleben gegenüber Bevacizumab in Kombination mit Standardchemotherapie bei triple-selektierten (RAS-WT/BRAF-WT und MSS/MSI-L-Status [MSS (Microsatellite Stable) / MSI-L (Microsatellite Instability-Low)])
mCRC-Patienten und Patientinnen mit linksseitigem Tumor.3
Zusätzlich zur Primäranalyse wurde die Biomarkeranalyse konzipiert, um die Wirksamkeit der Therapieregime bei
mCRC-Patienten und Patientinnen mit klinisch relevanten molekularen Biomarkern zu untersuchen.3,7,8,9 Die Patient:innen wurden bei Studieneinschluss mittels Gewebeprobe auf RAS-WT vorselektiert, gefolgt von einer zusätzlichen Liquid Biopsy Analyse der im Plasma zirkulierenden Tumor-(ct)DNA vor Therapiebeginn. Hierbei wurde auf folgende genetische Variationen getestet: Mutationen in den Genen RAS (KRAS, NRAS), BRAF (V600E), eine Mikrosatelliteninstabilität (MSI), Alterationen in PTEN oder EGFR (extrazelluläre Domäne), Amplifikation von HER2, MET und ALK sowie auf RET- und NTRK-Fusionen.3
Bei triple-selektierten Patient:innen (RAS-WT/BRAF-WT und MSS/MSI-L-Status) mit linksseitigen Tumoren ergab sich ein medianes Gesamtüberleben (mOS) von 40,6 Monaten unter Vectibix® + mFOLFOX6 vs. 34,8 Monaten unter Bevacizumab + mFOLFOX6.3
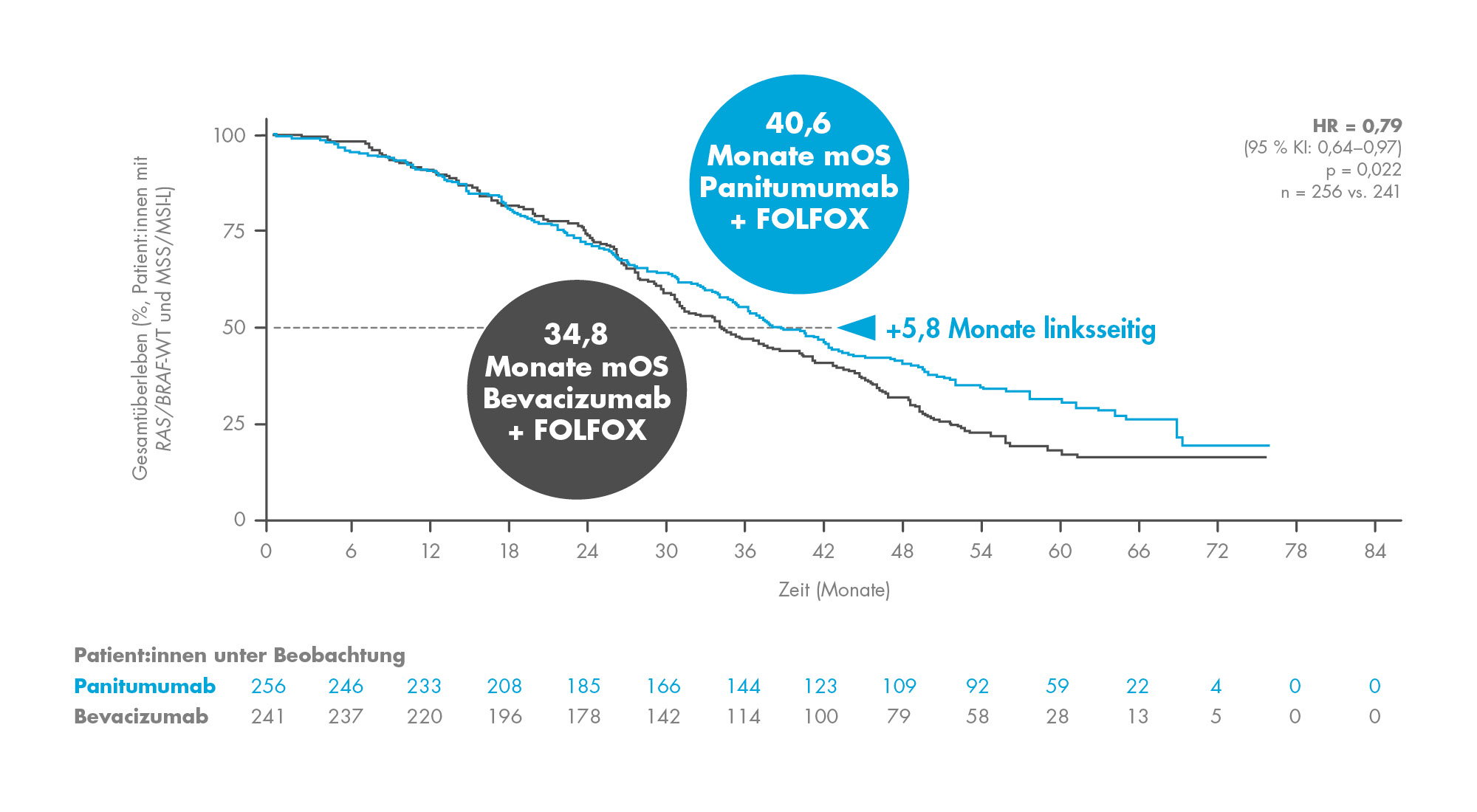

Abb. 1: Klinische Wirksamkeit beim linksseitigen mCRC nach Triple-Selektion: Medianes Gesamtüberleben (mOS) von 40,6 Monaten unter Panitumumab + mFOLFOX6 vs. 34,8 Monate unter Bevacizumab + mFOLFOX6 (Kaplan Meier Kurven). Mod. nach [3].
Auch triple-selektierte Patient:innen mit rechtsseitigen Tumoren profitierten hinsichtlich des medianen Gesamtüberlebens von der Kombination Vectibix® + mFOLFOX6. Das mOS im Vectibix®-Arm betrug 37,9 Monate und im Bevacizumab-Arm 30,9 Monate.3
Kurze Infusionszeit** und gute Infusionsverträglichkeit#,1
Vectibix® kann sowohl für die Patient:innen als auch das medizinische Fachpersonal eine spürbare zeitliche Entlastung im Behandlungsalltag bieten.
Das 14-tägige Dosierungsintervall und die kurze Infusionsdauer von nur 30 Minuten** kann eine effiziente Therapiedurchführung ermöglichen. Zudem enthält die Fachinformation keine verpflichtenden Angaben zu einer routinemäßigen Prämedikation oder Nachbeobachtung, was die Behandlung zusätzlich vereinfacht und patient:innenfreundlicher gestaltet. Diese Aspekte können zur Lebensqualität der Patient:innen beitragen.1


Die gute Infusionsverträglichkeit von Vectibix® lässt sich unter anderem auf den vollhumanen Antikörper-Typ zurückführen und konnte in klinischen Studien zur Monotherapie und Kombinationstherapie beim mCRC nachgewiesen werden. In einer Patient:innenpopulation von über 2000 Patient:innen (n = 2.224) betrug der Patient:innenanteil mit Infusionsreaktionen 1%, der Anteil mit Infusionsreaktionen von Grad 3 und 4 0,3%.1


* Vectibix® ist indiziert zur Behandlung von erwachsenen Patienten mit metastasiertem kolorektalem Karzinom (mCRC, metastatic colorectal cancer) mit RAS-Wildtyp: in der Erstlinientherapie in Kombination mit FOLFOX oder FOLFIRI; in der Zweitlinientherapie in Kombination mit FOLFIRI bei Patienten, die in der Erstlinientherapie eine Fluoropyrimidinhaltige Chemotherapie erhalten haben (ausgenommen Irinotecan); als Monotherapie nach Versagen von Fluoropyrimidin-, Oxaliplatin- und Irinotecan-haltigen Chemotherapieregimen.1
**30-60 Minuten, wenn die 60 Minuten-Erstinfusion toleriert wird.1
# Klinische Studien zur Monotherapie und Kombinationstherapie beim mCRC (n = 2.224), Patient:innenanteil mit Infusionsreaktionen: 1 %, Patient:innenanteil mit Infusionsreaktionen von Grad 3 und 4: 0,3 %.1
## Bei Therapieziel Tumorschrumpfung
Referenzen:
1. Fachinformation Vectibix®.
2. Boeckx N et al. Ann Oncol 2017;28(8):1862-1868.
3. Yamazaki K et al. J Clin Oncol 2023;41(suppl 16; abstract 3508).
4. Douillard JY et al. Eur J Cancer 2015;51(10):1231-1242.
5. Carrato A et al. Eur J Cancer 2017;81:191-202.
6. Herrero FR et al. Ann Oncol 2017;28(suppl 5) und Poster 519P.
7. Watanabe J et al. JAMA 2023;329(15):1271-1282.
8. Morris VK et al. J Clin Oncol 2023;41(3):678-700.
9. Cervantes A et al. Ann Oncol 2022;34(1):10-32.
DEU-954-0725-80011
Amgen GmbH
Firmensitz
Riesstraße 24
80992 München
Telefon: (0 89) 149 096-0
Telefax: (0 89) 149 096-2000